Viedoc的概述
本课提供的是关于Viedoc系统的概述包括功能和对于系统架构(应用,语言,环境和许可)
简介
Viedoc是一项基于互联网系统用于管理临床试验中病例报告表(CRF)数据和病人注册的服务。
Viedoc是一个可以用于数据收集,管理,验证以及展示临床试验数据的EDC系统。Viedoc作为一个SaaS(Software as a Service软件即服务)可直接使用 浏览器而无需任何安装。使用时非常直观并且具有用户友好的界面使其能更高效地分享信息。
Viedoc是一个以研究为中心的系统,比如:所有的功能或多或少都为了一个具体的研究项目而服务。通常一个在Viedoc中的研究项目是一个临床试验或是当有数据收集需求的其他项目。
Viedoc的一些主要的功能:
- 数据处理:
- 病人筛选
- 随机
- 在线数据输入 (eSource依从)
- 自动数据传输
- 数据签名
- 注解
- 医学编码
- 文件上传
- RTSM
- 随机和高级分配功能
- Viedoc Logistics
- 数据导出:
- 导出的格式:
-
Microsoft Excel - Office Open XML
-
CSV - Comma-separated values
-
PDF - PDF Archive
-
CDISC ODM - XML
-
- 自动创建空白病例CRF和注释CRF
- 稽查轨迹
- 数据质量参数
- 研究统计
- 导出的格式:
- 数据审核/监察:
- 原始资料核对 (SDV)
- 临床/ 数据的审核和锁定
- 预质疑和质疑处理
- 其他:
- Single point of login
- 24/7技术支持
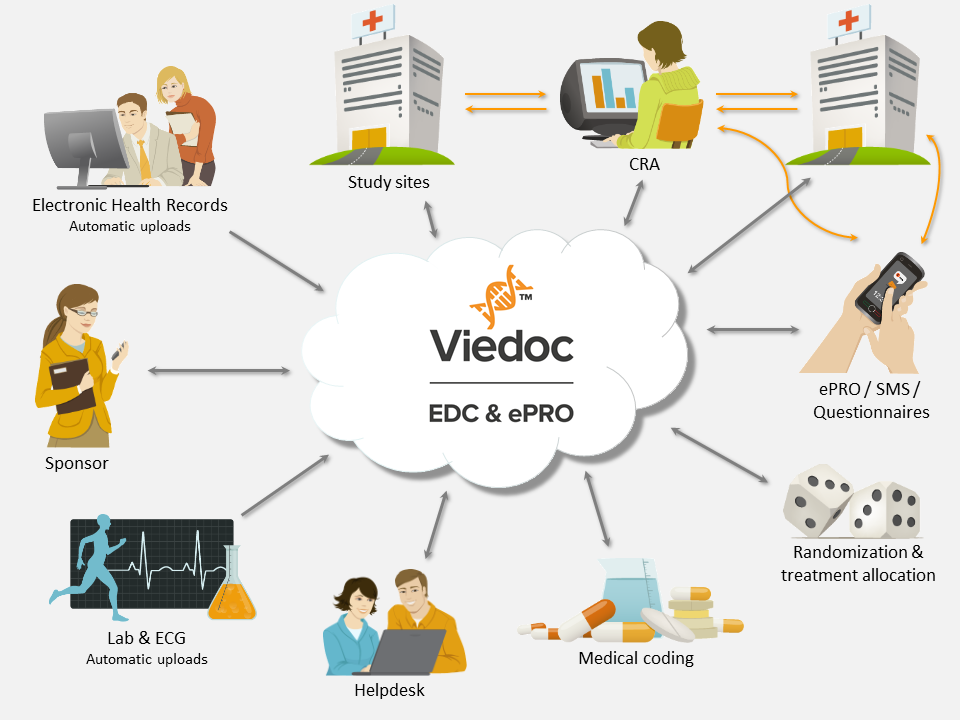
下图是主要的Viedoc交互和功能概述:
Viedoc符合相关的欧洲、北美以及日本的指导原则和法规:
- 21 CFR part 11
- ICH-GCP
- CDISC
- Personal Data Privacy Act and EU Annex 11
- CSUCI
- HIPAA
- Developed according to GAMP 5
- GDPR
Viedoc中的临床研究
研究中心
每个临床研究至少有一个相应的中心来对应相应的医疗机构。每个Viedoc的用户对于同一个研究项目可以有进入一个或多个中心的权限同时也可以有进入一个或者几个研究项目的权限。每个Viedoc的用户都能通过用户角色和研究相关联。同一个用户在同一个研究中心中可以有一个或者多个角色,也可在不同的中心中有不同的角色。
访视和表单
每个研究中的受试者的数据都有一些问题需要回答和完成。每个表单中可以收集一系列的问题。表单可以设计在访视中也可不设计在访视中(日志表和计划外访视)。访视相关表单与特定访视相关联,而其中的数据是在临床试验过程中发生的或者与其相关的。而访视不相关表单可以用于报告数据和事件不论是发生之前、之中或是访视之后。举例来说,病史 ,合并用药或者不良事件可记录在访视不相关表单。
受试者
所有研究的受试者都会有一个唯一的受试者编号,除了这个受试者编号,病人可使用不同的背景信息来识别比如性别、缩写或者生日。受试者的背景信息通常在添加病人时录入并且在研究进程中很少会改变。
系统构架
Viedoc的平台
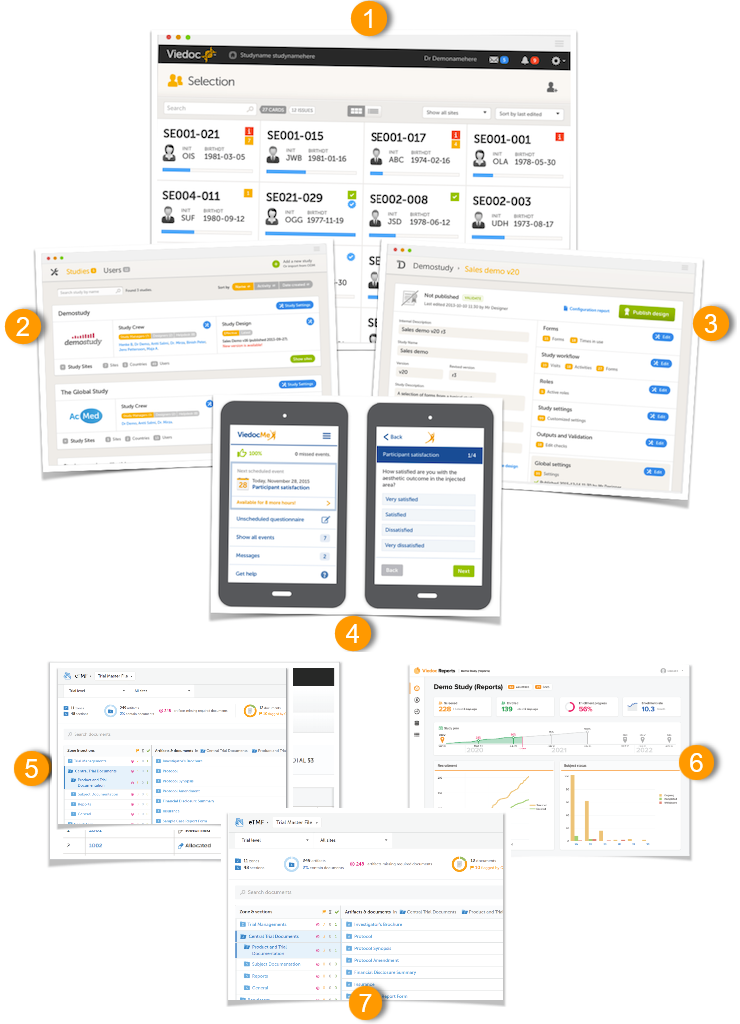
Viedoc的平台由以下七个不同的应用所构成:
- Viedoc Clinic -供进入CRF权限的研究中心用户和项目组成员使用
- Viedoc Admin - 供研究中需要管理用户、中心以及研究设计更新的成员使用。Viedoc Admin是您开启一个新的研究项目、管理进行中的项目和结束完成的项目的互动平台。
- Viedoc Designer - 供项目中设计研究的开发人员使用。Viedoc Designer是你可以设计表单、设置研究流程、增加角色、准备随机化、增加逻辑核查等功能的部分 。
- Viedoc Me -受试者日志或者电子化患者报告结果(ePRO)。所有的受试者问卷都可以非常容易通过ViedocMe完成和递交。
- Viedoc Logistic - 适用于处理你们的研究药物管理。
- Viedoc Report - 用于查看和分析研究进度和表现。
- Viedoc TMF - 用于收集,管理,分享和储存您的研究项目的重要文档的电子库。
- Viedoc Coder - 用于医学编码
eLearning语言
Viedoc Learning 是一套用户指南合集,旨在为使用我们各类产品、担任不同角色、使用各项功能的用户提供支持。完整的用户指南列表可在以下位置查看:Viedoc Learning Directory
组织
Viedoc里的研究依靠组织来分组的:举例来说,每个客户都拥有各自的组织来“存放”其研究项目。每个组织都有一个默认的到管理员。接受过培训的Viedoc的产品专员有责任会为相应组织的用户提供权限并且可以在平台中增加新的研究项目。
| 重要!组织的管理员需要负责给组织中不同的用户得到他们相应的培训。 |
系统环境
作为Viedoc客户,您会得到两个不同的系统环境:一个用来作为测试库而另一个作为正式库。不同的两个环境可以让您在特定的研究合同签订前更好地评估和使用Viedoc。
项目需要在测试库的环境中开始并且进行测试,推入正式库后,正式库的环境就可以分享给申办方和外部用户。值得注意的是只要在正式库环境中添加一个培训类型的中心,就可以将一个研究设置为在演示版下运行。
请注意!请不要混淆正式库中的演示版和测试库。演示版的目的是允许中心人员访问特定的培训中心,以便在访问正式库数据之前对系统有足够的了解。当一个研究在正式库的演示版和正式版中都添加了中心,在Viedoc Clinic中,您将能看到一个转换开关来转换模式比如:演示版或者正式版。
研究和(或)研究设计可以很容易地从一个环境通过CDISC ODM导出和导入功能转到另一个环境。
您需要联系您的组织管理员来获得您相应的权限。
请注意! 我们不能保证在测试环境下运行的研究项目可以完全和持续地备份 ,所有请不要用测试环境来录入研究正式数据。
许可
所有研究进入正式库前都需要有一个许可号。这个许可证将由Viedoc代表所提供。这个许可费将由以下因素所决定:研究时常,中心数量,病人数量等 。许可费将从加入首个病人开始直到研究在Viedoc里被锁定。 如果研究在锁库后两个月内未被删除将会产生锁库后费用。
每个许可证都会有个许可号。许可号您可在 Work Order 中找到,在Viedoc Admin中研究设置中有处内部参考编号,请在此处填写许可号。(图 1)。
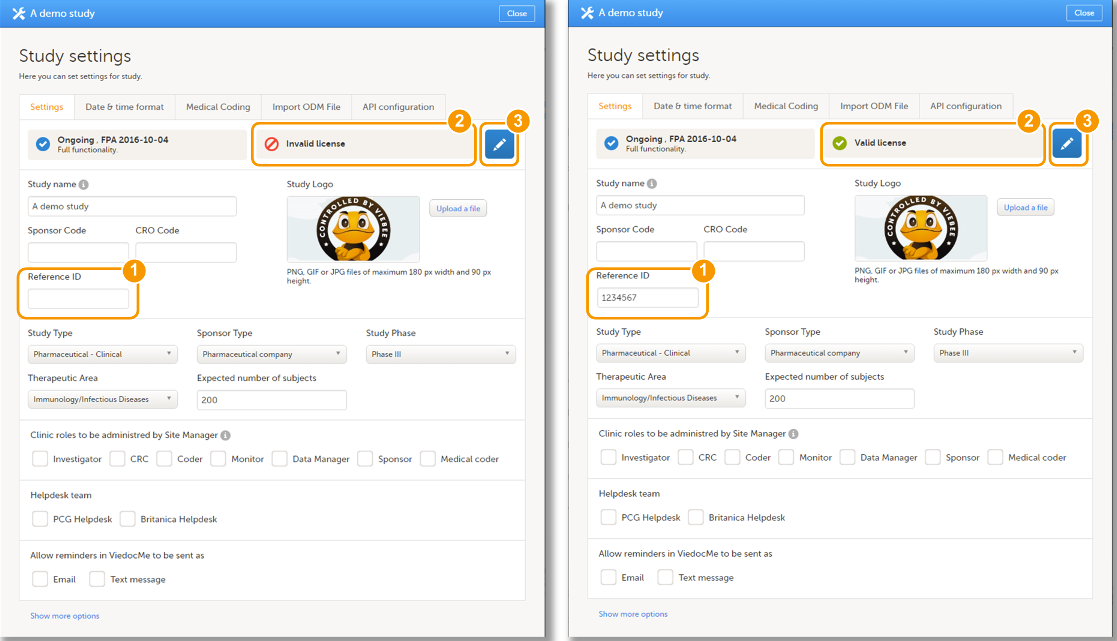
在内部参考编号处填写许可号可以验证您的许可号。如果许可号是有效的, "许可有效"的字样将会出现在以下几个部分:
- Viedoc Admin中的研究设置 (图2),
- Viedoc Admin中的研究列表
- Viedoc Admin中的研究状态 (图 3)。
完成了许可号的验证,研究就拥有正式版了。只要一个“正式版”的中心在正式库中添加完成,这项研究就正式上线,与此同时,参考号就被锁定之后也不能解锁更改了。
如果您希望得到更多关于许可和参考号的信息,请联系您的Viedoc代表。
版本说明
有关新增功能、功能更新及漏洞修复的相关信息,可在版本说明中查阅,该文件可从 Viedoc 官网下载:
- https://www.viedoc.com/support/release-notes for the international website
- https://www.viedoc.co.jp/support/release-notes/ for the Japanese website
- https://www.viedoc.cn/support/release-notes/ for the Chinese website
