研究开始页面
简介
当您点击项目图标进入登录页面, 项目开始页面会加载,加载页面如下图所示,每个图标包含了不同的功能,逐个点击每个图标,您讲更好的了解当前项目的信息。
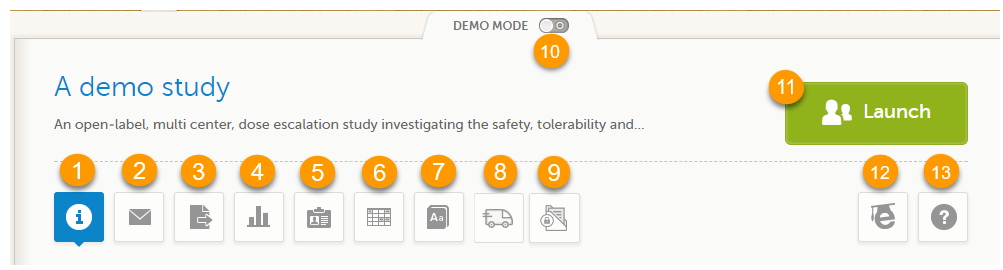
1. 研究状态
2. 信息
3. 数据导出
4. 参数
5. 角色
6. 参考值
7. 医学编码
9. Viedoc eTMF
10. 演示模式
11. 开始
12. eLearning/文档和培训
13. 技术支持
注意! 导出,参数,医学编码,演示模式和开始的图标只会在您有权限的时候显示。您是否有权限,取决于您的角色以及您的角色是否有该权限。角色和权限可以在研究设计中进行定义。
第一页您能查看到您选择的研究的文档和培训:
- 如果您有必读文档,您将会打开文档和培训。
重要!所有必读文档都在您进入研究前需要被勾选,若研究经理选择演示模式不需完成培训,则您可进入演示模式。
若您没有任何需要签名的必读文件,第一页就会显示研究状态页。
研究状态
您能在第一页看到一些研究进度的基本信息 - 研究,国家或者中心层面的进度(取决于您是否有权限查看所有中心):

您可以筛选国家或者中心:

您可在本页查看以下信息(取决于您查看中心的权限):
- 问题:
- 已回答的质疑 - 所有已回答质疑的数
- 未回答质疑 - 所有未回答质疑数
- 表单 - 所有有问题的表单
注意!对于已解决和未解决的质疑,这仅包括手动质询和验证质疑,不包括缺失数据质疑。对于已解决的质疑,包括以下状态:已解决、已拒绝、已批准、已关闭。
- 审核:
- 监查进度% - 监查员已确认临床审核表单/所有可以确认临床审核表单的百分比。
- 数据管理进度% - 数据经理已确认数据管理审核表单/所有可以确认数据管理审核表单的百分比。
- 源数据审核% - 监查员已完成源数据核查表单/所有需要做源数据审核表单的百分比。
- 确认:
- 研究者签名% - 研究者已电子签名表单/所有可以电子签名表单的百分比。
- 质疑进度% - 已确认质疑/所有需要确认的质疑的百分比。 若您想要了解质疑状态和过程,请详见质疑概述。
- 已锁定表单进度% - 已锁定表单/所有填写表单的百分比。
- 我的统计:
- 已添加受试者 - 总添加受试者数。
- 第一名受试者添加日期 - 添加第一名受试者的日期。
- 最后一名受试者添加日期 - 上一次添加受试者的日期。
请注意! 所有的数据都和模式选择(演示/正式),演示模式只显示演示模式的数据。
信息
这里的信息可以是您账户相关的系统信息(例如关于密码过期的提示)或者当前研究的信息(例如eCRF的变更-更多内容,请见确认研究设计的变化,或者其他来自研究配置的信息)
在消息栏内,蓝色的圆点代表项目层级的提醒,橙色的圆点代表CRF更新等待中心审阅,红色的圆点代表密码即将过期。
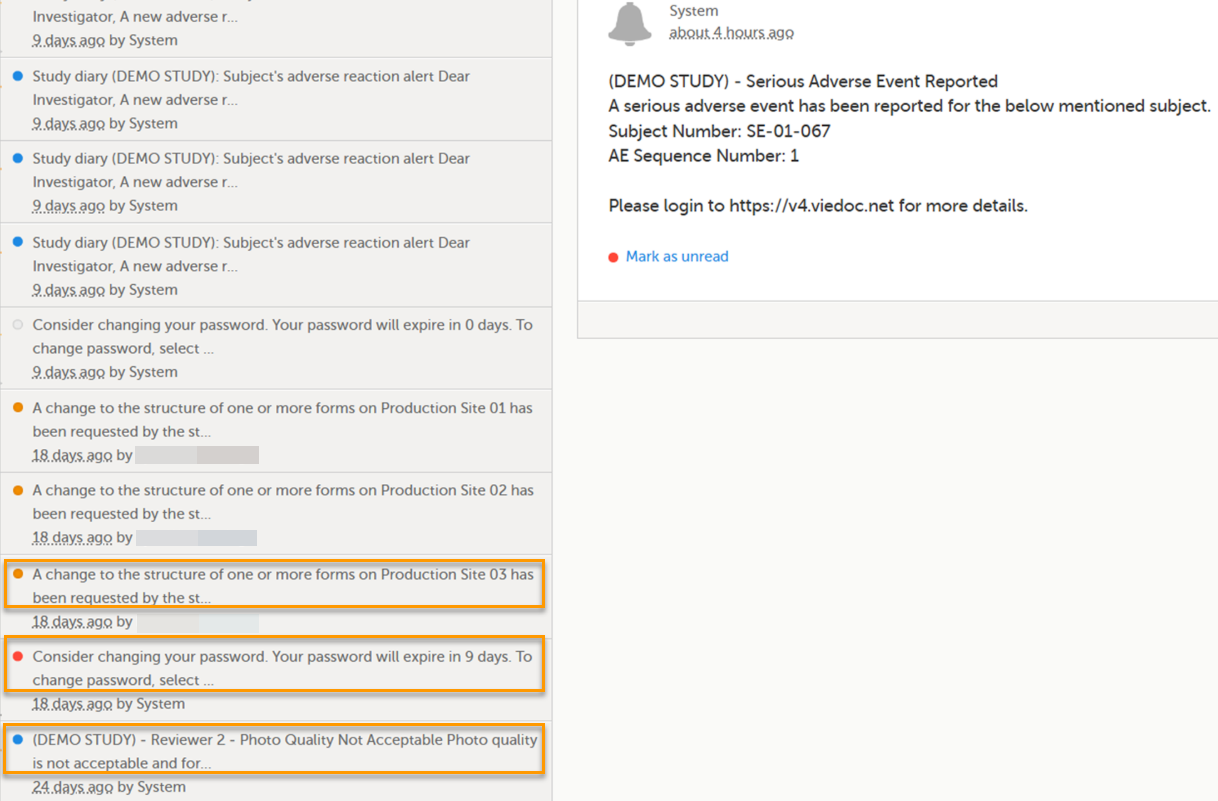
不同颜色的圆点将会告诉您是否有信息未读。

提醒信息
根据研究设置,您可以收到关于研究中数据发生重要变化的相关提醒。(例如,当发生严重不良反应时)这样的提醒可以通过信息或者邮件接受。
根据研究设置,提醒的邮件中可能包含触发该提醒的表单的PDF格式文件作为附件。
如果通过密码保护邮件提醒附件中的内容的设定在当前研究中被启用了,那么您需要首先知道打开附件中文档的密码才能浏览该附件。这一密码将由您的研究管理员(Study Manager)提供。
当您收到包含了附件被密码保护的邮件提醒时,您在打开该附件时将会看到下图中的弹窗。您可以在此输入密码:
数据导出
数据导出包括以下的格式:
- Excel
- CSV
- SAS
- CDISC ODM
请注意! 并不是所有用户都有数据导出的权限。
若您需要更多信息,请见导出数据。
参数和Viedoc Reports
参数的功能可以给您一个未解决质疑和缺失数据的概览。
请注意!并不是所有用户都有查看参数的权限。
若您需要更多信息,请见参数。
如果Viedoc Reports包含在研究许可证中并已启用,则可以通过Metrics模块访问它。有关更多信息,请参见启动Viedoc Reports。
角色
角色页面可提供以下信息:
- 您有权限的角色,请见我的角色。
- 您所有有权限的中心,请见可用的角色和用户身份。
我的角色
在我的角色页面您在项目中的角色:
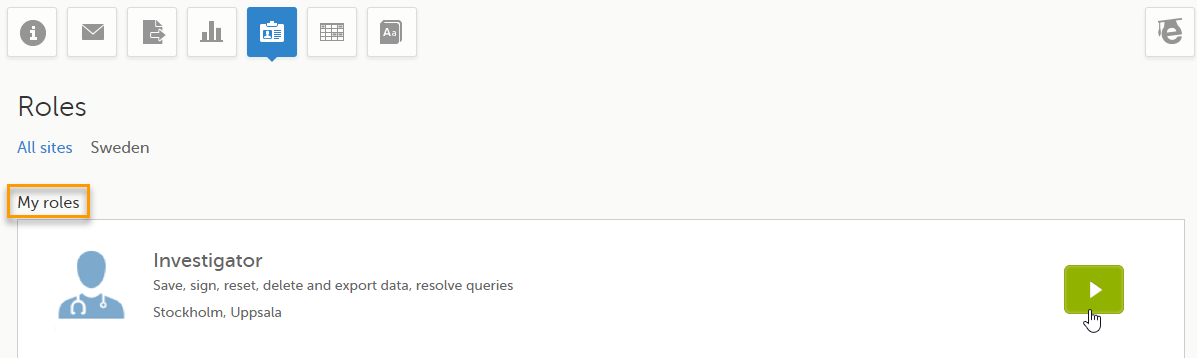
如下信息会被陈列:
- 角色名 (比如研究者)
- 权限 (比如保存,签字,重置/删除/导出数据和解决质疑)
- 您有权限的中心
点击右侧绿色箭头,您会进入项目的选择页面。这和点击开始页面是一样的效果。
可用的角色和用户身份
在这个部分,您可看到您拥有权限的中心的所有角色和用户:
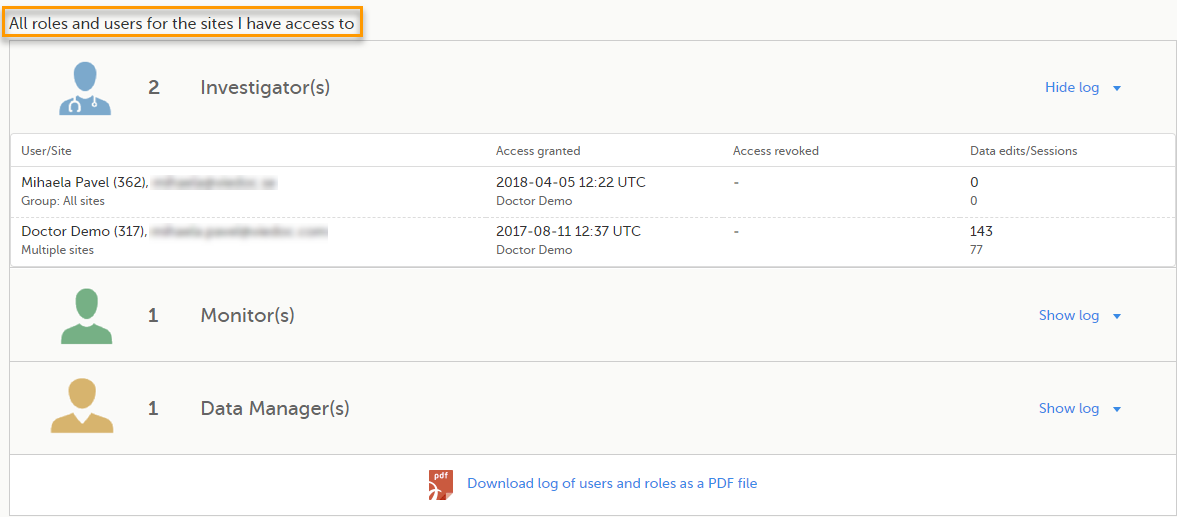
若您想查看更详细的角色信息,点击显示记录,您可看到如下信息:
- 用户/中心 - 用户名,邮件和中心。
- 权限已授予 - 授予时间(UTC时间)和由谁用户名授予。
- 权限已撤销 - 撤销时间(UTC时间)和由谁用户名撤销。该列只在权限被撤销情况下会显示内容。
- 数据修改/会话 - 用户编辑数据次数和总登录次数(进入该研究项目)。
*UTC时区的日期和时间。
用户日志
在每个研究当中,您可以下载PDF或Excel格式的您有权限的中心的所有用户和角色信息日志。生成的文档会使用您目前用于浏览Viedoc页面的语言呈现该国家/中心的信息。
注意!
- 在Viedoc Clinic,日志中包括正式研究中心和演示研究中心以及这两种研究中心的角色/用户信息。
- 日志中包含研究的系统角色(不包括组织层级用户)。
- 当为正式研究中心生成日志时,演示研究中心的研究中心管理员也会被纳入日志,因为研究中心管理员属于系统角色。
您可以通过在研究起始页底部选择生成PDF文件/生成Excel文件,生成当前Viedoc语言版本的国家/研究中心选择日志:

一旦生成过用户日志,您可以:
- 下载上次生成过的该国家/中心的记录 - 对于当前的国家/中心选择,服务器上会备份上次生成的记录 (显示生成时间和日期)。您可以节约再次生成的时间。或者
- 点击再次生成文档 - 若您想要最新的日志。

用户和角色日志的PDF报告
PDF用户和角色日志包括以下章节:
- 总结 - 激活/失活的角色,激活/失活的用户和参与数据录入的人员都以中心来分组。
- Active Role 是指所有活跃用户在某一研究中心当前持有的角色。
- Inactive Role 是指曾被分配过、但当前无任何活跃用户持有的角色。
- Active User 是指至少有一个活跃角色的用户。
- Inactive User 是指曾在某一研究中心拥有至少一个角色,但该研究中心的所有角色均已被撤销的用户。
- 角色 - 每个角色的权限和相应的历史记录都以中心来分组。
- 各中心的用户日志 - 所有有权限接触数据的用户包括用户活动都以中心来分组。
- 账户日志 - 上述用户账户的改变记录以中心组来分组。(以用户ID区分)。
用户管理日志的Excel报告
您可下载用户管理日志的Excel报告,报告中包括您有权限的中心的所有用户和角色的信息,用户管理日志包括以下内容:
- 报表信息 - 关于何时由和人生成本日志,一些本研究项目状态相关的概要信息。以及下列更多详细信息:
- 组织名称
- 研究名称
- 正式研究的GUID
- 演示研究的GUID
- PMS 研究:申办方侧的生产研究的GUID
- PMS 研究:申办方侧的演示研究的GUID
- 用户权限日志 - 本列表分行显示每个中心的所有角色的具体用户权限信息,既包括Clinic角色也包括系统角色。关于本列表上其他列具体内容的一些解释如下:
- 中心组 - 代表该用户是通过中心组的方式获得权限邀请。可包括下列值:培训中心,国家或者所有中心。
- 2FA - 代表该用户拥有何种等级的双重验证。可包括下列值:研究等级,账户等级,或者未激活双重验证。
- 最近一次系统登录日期/时间 - 每个用户的最近一次登录系统的信息(仅适用于终端用户,不适用于API客户端用户)
- 认证 - 代表用户是否收到该角色的认证。可包括下列值:是,否或为空(当该角色没有必修培训时)。
- 如果用户签名确认获得了其角色要求的培训的认证,这一列将显示:Certified:Yes。
- 如果用户仅确认阅读并理解,但还未签名确认获得认证,这一列将显示:Certified:No。
- 用户类型 - 代表用户的类型。可能的值有:End User 或 API Client,以说明该用户是可登录系统的终端中户还是一个Web API 客户端角色。
- 用户邀请日志 - 包含待处理邀请和已拒绝邀请信息的列表,包括临床角色和特殊角色。本工作表中的某些列将在此处进一步解释:
- 角色 - 受邀用户的角色。
- 电子邮件地址 - 每个受邀用户的电子邮件地址。
- 现有用户 - 指示受邀用户是否已经在研究项目中拥有其他角色或是新用户。可能值“是”、“否”。
- 初始邀请发送日期/时间 - 涉及每个用户的首次邀请信息
- 发送初始邀请的用户的ID - 用户的数字用户ID
- 用于发送初始邀请的显示名称 - 发送初始邀请时该用户在Viedoc系统中使用的对应用户的显示姓名。
- 用于发送初始邀请的电子邮件地址 - 为受邀用户发送初始邀请的电子邮件地址。
- 邀请重新发送次数 - 邀请被重新发送的次数。
- 最新邀请发送日期/时间 - 涉及每个用户的最新邀请信息。
- 状态 - 邀请状态,可能包括“待处理”、“已拒绝”。
- 拒绝邀请的日期/时间 – 关于每个用户的已拒绝邀请的信息。
- 证书日志 - 用户的证书列表。在 Viedoc 4.65版本之前授予的证书不包含该证书被授予的角色的信息,即,“授权角色”格将为空。
- 总结 - 总结包含各中心用户的国家,中心编号,中心名,激活/失活用户数以及最近一次登录的日期/时间等信息。
- 账户设定日志 - 所有账户设定的变更记录,包括:用户ID,变更记录,用户名和变更日期/时间。
参考值
当您点击参考值图标,您能查看到一系列参考值源 - 相关联的范围(例如实验室)也显示在此。您可打开参考值编辑器。详情请见 使用参考值。
请注意!并不是所有用户都有查看参考值的权限。
医学编码
医学编码功能能让您编码医学事件例如不良事件,病史和合并用药。当您点击医学编码图标,您可查看相关参数与需要编码的范围。
请注意!并不是所有用户都有查看医学编码的权限。
若您需要更多的医学编码的权限,请见医学编码。
Viedoc Logistics
Viedoc Logistics是用于管理您的研究药物供应的界面。 使用Viedoc药物物流系统需要有效的许可证。有关Viedoc Logistics的更多信息,请参见 Viedoc User Guide for Supply Managers。
Viedoc eTMF
Viedoc eTMF是一个用于获取、管理、共享和存储基本文档的数字存储库。
有关Viedoc eTMF的更多信息,请参见Viedoc eTMF用户指南。
演示模式
研究可以设置有演示模式。您可选择演示版和正式版使用:

演示按钮只在您有两个版本都有权限时会显示。
演示按钮会告诉您演示版本在使用中,请不要在演示版本中录入任何正式数据!
您可查看视频教程激活演示版。
开始
点击开始您就能进入受试者数据和eCRF。
当您有Viedoc Clinic的权限时,您就能点击开始按钮。
如果在一个研究项目中,您有多个角色,您会需要在进入时选择角色。
eLearning/文档和培训
如果您有必读文档和必做培训需要阅读和签字,进入项目后,您会直接看到本页。
在这个部分中您可查看到被分配给您的eLearning和文档。更多关于文档和证书的内容,请见文档和培训。
Viedoc Clinic 用户指南现在有以下语言:
- 英语
- 中文(简体)
- 日语
若您需要修改Viedoc用户指南的语言,当您打开后,请在右上角点击语言的选项,请看下图:

小提示!eLearning的课程您可下载PDF并打印,您可装订在研究者手册中。
技术支持
点击支持图标,您将能查询到帮助支持的信息。通常来说,您会看到中心监查员的信息,因为一般监查员是中心的第一联系对象。
